565
565
Dernières publications
L’Arabe est la Xème langue parlée au monde avec plus de 400 millions de locuteurs. Elle est également la langue officielle de XX pays, depuis la Mauritanie jusqu’à Oman, en passant par l’Égypte. Cependant, est-ce que l’on parle le même arabe en Afrique sub-saharienne et en Syrie. Clairement, non. L’Arabe est une langue versatile qui se ramifie en de nombreux dialectes. Avec ses variétés...
Pourquoi challenger son agence de traduction régulièrement ? Challenger un fournisseur est une bonne pratique et synonyme d’une bonne hygiène de gestion : éviter la complaisance, vérifier la valeur réelle, et s’assurer que le service suit l’évolution de vos besoins. C’est valable pour toutes les entreprises et tous les types de fournisseurs. Même lorsque la relation commerciale paraît excellente...
Nous en avons déjà parlé à travers de nombreux blogs : la traduction dans le cadre du règlement MDR UE 2017/745 entourant les dispositifs médicaux n’est pas une simple étape finale. C’est un élément à part entière de la conformité, qui a attrait à la sécurité d’utilisation en tant qu’elle affecte directement le contenu de la documentation fournie avec un DM. C’est exactement pour cela que la...
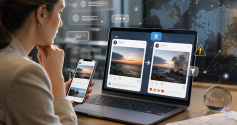
Depuis quelques mois, la traduction automatique s’impose progressivement comme une fonctionnalité par défaut sur les réseaux sociaux, modifiant en profondeur la manière dont les contenus sont perçus et compris par les utilisateurs. Conçue pour faciliter l’accès à l’information, elle peut pourtant altérer le sens des messages lorsqu’elle est activée sans contrôle. Selon Clubic, un média spécialisé...
Déjà en 2022, le phénomène BookTok avait enregistré des vues considérables, on compte près de 1,6 milliard de vues pour environ 376 000 vidéos produites portant le mot clé #BookTok, selon Actualitté, la presse professionnelle spécialisée dans l’édition. Ce phénomène de lecteurs apparu sur la plateforme TikTok, exerce aujourd’hui une influence majeure sur l’industrie du livre. Lorsqu’un ouvrage...
La question revient sans cesse chez les fabricants, les importateurs, les distributeurs, les PRRC et les équipes qualité/réglementaire : la traduction par l’IA est-elle autorisée ou non selon le règlement MDR (UE) 2017/745 ? Réponse courte : oui, l’usage d’outils d’IA est autorisé pour les traductions, mais son utilisation est encadrée et conditionnée. Dans la pratique, certains auditeurs ou...
L’IA générative a fait irruption dans les pratiques de traduction à une vitesse qui dépasse les cycles habituels de réforme des programmes. En quelques mois, des outils capables de reformuler, résumer, adapter un ton ou produire une traduction apparemment convaincante se sont installés dans les usages étudiants comme professionnels. Cette évolution ne change pas seulement les outils disponibles...
Dans les secteurs réglementés, la traduction engage la conformité, la sécurité d’utilisation et, parfois, la responsabilité de l’entreprise. C’est précisément pour sécuriser cette chaîne de valeur que la norme ISO 17100 a été créée et publiée en 2015. Depuis, elle et s’est imposée comme un repère international. En 2026, après d’existence une question peut légitimement se poser : la norme ISO...
L’IA et la traduction ne forment plus un duo « expérimental » : elles deviennent le moteur d’une reconfiguration profonde de l’industrie de la traduction et, plus largement, de l’industrie linguistique. Ce basculement ne se résume pas à « traduire plus vite ». Il change la manière dont les organisations achètent des solutions linguistiques, dont les prestataires se structurent, et dont la valeur...
En 2026, beaucoup d’acheteurs imaginent encore une entreprise de traduction comme un atelier rempli de traducteurs salariés. En réalité, la structure fournisseur de services linguistique moderne ressemble plutôt à un centre de pilotage : la production est largement externalisée, tandis que la coordination et l’assurance qualité sont internalisées. Ce virage s’est amorcé à partir des années 2000...
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- …
- suivante ›
- dernière »